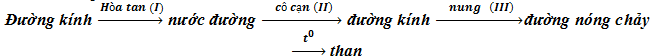Đề kiểm tra 45 phút chương II: Phản ứng hóa học
Cập nhật lúc: 15:00 21-06-2016 Mục tin: Hóa học lớp 8
Xem thêm:
ĐỀ KIỂM TRA 45 PHÚT CHƯƠNG 2: PHẢN ỨNG HÓA HỌC
ĐỀ BÀI
Phần I: Trắc nghiệm khách quan. ( 4 điểm)
Hãy khoanh tròn vào một trong các chữ cái A, B, C hoặc D đứng trước câu trả lời đúng nhất
Cho các hiện tượng:
1. Hòa tan muối ăn vào nước được nước muối.
2. Khi đánh diêm có lửa bắt cháy.
3. Thanh đồng được kéo thành sợi nhỏ để làm dây điện.
4. Thuỷ tinh được đun nóng chảy ở to cao rồi thổi thành bóng đèn, lọ hoa, cốc …
5. Cho 1 mẫu đá vôi vào giấm ăn thấy có bọt khí thoát ra.
Câu 1: Hiện tượng vật lí là
A. 1, 3 và 4 B. 1 và 2
C. 2 và 3 D. 2 và 5
Câu 2: Hiện tượng hóa học là
A. 1, 3 và 4 B. 1 và 2
C. 2 và 3 D. 2 và 5
Câu 3: Phát biểu đúng là
A. Làm muối từ nước biển là sự biến đổi hóa học.
B. Thức ăn bị ôi thiu là sự biến đổi vật lí.
C. Nung đá vôi là sự biến đổi hóa học.
D. Cồn để trong lọ không kín bị bay hơi là sự biến đổi hóa học.
Câu 4: Cho quá trình sau:
Giai đoạn có sự biến đổi hóa học là
A. I B. II C. III D. IV
Câu 5: Phát biểu sai là
A. Trong 1 PƯHH, tổng khối lượng các chất sản phẩm bằng tổng khối lượng các chất tham gia.
B. Trong 1 PƯHH, số phân tử của các chất được bảo toàn.
C. Trong 1 PƯHH, số nguyên tử của mỗi nguyên tố được bảo toàn.
D. Trong 1 PƯHH có n chất nếu biết khối lượng của (n-1) chất thì tính được khối lượng của chất còn lại.
Câu 6: Lưu huỳnh cháy theo sơ đồ phản ứng sau: Lưu huỳnh + khí oxi → khí sunfurơ. Nếu đã có 48g lưu huỳnh cháy và thu được 96g khí sunfurơ thì khối lượng oxi đã tham gia phản ứng là
A. 40g B. 44g C. 48g D. 52g
Câu 7: Thủy ngân oxit bị phân huỷ theo sơ đồ sau:
Thuỷ ngân oxit → Thuỷ ngân + Oxi. Khi phân huỷ
2,17g thuỷ ngân oxit thu được 0,16g oxi. Khối lượng thuỷ ngân thu được trong thí nghiệm này là
A. 2g B. 2,01g C. 2,02g D. 2,05g
Câu 8: Một cốc đựng dung dịch axit clohidric và 1 viên kẽm được đặt ở đĩa cân A. Trên đĩa cân B đặt các quả
cân sao cho kim cân ở vị trí cân bằng. Bỏ viên kẽm vào cốc axit. Biết rằng có phản ứng:
Kẽm + axit clohidric → Kẽm clorua + khí hidro. Vị trí của kim cân là
A. Kim cân lệch về phía đĩa cân A. B. Kim cân lệch về phía đĩa cân B.
C. Kim cân ở vị trí thăng bằng. D. Kim cân không xác định.
Câu 9: Khí Nitơ và khí Hidro tác dụng với nhau tạo ra Amoniac (NH3). PTHH viết đúng là
A. N + 3H → NH3 B. N2 + H2 → NH3
C. N2 + H2 →2NH3 D. N2 + 3H2 → 2NH3
Câu 10: PTHH cho biết chính xác
A. Số nguyên tử, phân tử của các chất tham gia phản ứng.
B. Tỉ lệ số phân tử (nguyên tử) của các chất trong phản ứng.
C. Khối lượng của các chất phản ứng.
D. Nguyên tố nào tạo ra chất.
Câu 11: Phản ứng giữa Fe2O3 và CO được biểu diễn như sau:
xFe2O3 + yCO → 2Fe + 3CO2.
Các giá trị của x và y cho phương trình cân bằng là
A. x = 1; y = 1 B. x = 2 ; y = 1 C. x = 1 ; y = 3 D. x = 3 ; y = 1
Câu 12: Cho PTHH: 2Cu + O2 → 2CuO. Tỉ lệ giữa số nguyên tử đồng: số phân tử oxi: số phân tử CuO là
A. 1:2:1 B. 2:1:1 C. 2:1:2 D. 2:2:1
Câu 13: Trong phản ứng hóa học, phân tử này biến đổi thành phân tử khác là do
A. Các nguyên tử tác dụng với nhau.
B. Các nguyên tố tác dụng với nhau.
C. Liên kết giữa các nguyên tử không bị thay đổi.
D. liên kết giữa các nguyên tử thay đổi.
Câu 14: Trong một phản ứng hóa học, các chất phản ứng và chất tạo thành phải chứa cùng
A. Số nguyên tử của mỗi nguyên tố. B. Số nguyên tử trong mỗi chất.
C. Số phân tử của mỗi chất. D. Số nguyên tố tạo ra chất.
Câu 15: Có phát biểu: “Trong PƯHH chỉ xảy ra sự thay đổi liên kết giữa các nguyên tử (1), nên tổng khối lượng các chất được bảo toàn (2)’’. Trong đó
A. (1) đúng, (2) sai.
B. cả 2 ý trên đều đúng và ý (1) giải thích cho ý (2).
C. (1) sai, (2) đúng.
D. cả 2 ý trên đều đúng và ý (2) giải thích cho ý (1).
Câu 16: Phương trình hóa học dùng để
A. Biểu diễn PƯHH bằng chữ.
B. Biểu diễn ngắn gọn PƯHH bằng công thức hoá học.
C. Biểu diễn sự biến đổi của từng chất riêng rẽ.
D. Biểu diễn sự biến đổi của các nguyên tử trong phân tử.
Phần 2: Tự luận (6 điểm)
Câu 17. Lập PTHH của các phản ứng sau, cho biết tỉ lệ số nguyên tử, phân tử của các chất trong mỗi phản ứng
a. Mg + HCl → MgCl2 + H2
b. Fe2O3 + CO → Fe + CO2
c. Al + H2SO4 → Al2(SO4)3 + H2
d. Al + Cl2 → AlCl3
Câu 18. Cho 8,4g bột sắt cháy hết trong 3,2g khí oxi (đktc) tạo ra oxit sắt từ (Fe3O4).
a. Viết PTHH của phản ứng và cho biết tỉ lệ số nguyên tử, phân tử của các chất trong phản ứng.
b. Tính khối lượng oxit sắt từ tạo thành.
Câu 19 . Nếu để một thanh sắt ngoài trời thì sau một thời gian khối lượng thanh sắt sẽ nhỏ hơn, lớn hơn hay bằng khối lượng ban đầu? Hãy giải thích.
ĐÁP ÁN VÀ THANG ĐIỂM
Phần I. Trắc nghiệm khách quan. (4 điểm)
Mỗi lựa chọn đúng đạt 0,25 điểm
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
|
A |
D |
C |
D |
B |
C |
B |
B |
D |
B |
C |
C |
D |
A |
B |
B |
Phần II. Tự luận (6 điểm)
|
Câu |
Đáp án |
Điểm |
|
Câu 1 (3 điểm) |
a. Mg + 2HCl → MgCl2 + H2 |
0,5đ |
|
Số nguyên tử Mg : số phân tử HCl : số phân tử MgCl2 : số phân tử H2 = 1:2:1:1 |
0,25 |
|
|
b. Fe2O3 + 3CO → 2Fe + 3CO2
|
0,5đ |
|
|
Số phân tử Fe2O3 : số phân tử CO : số nguyên tử Fe : số phân tử CO2 = 1:3:2:3 |
0,25 |
|
|
c. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2 |
0,5đ |
|
|
Số nguyên tử Al : số phân tử H2SO4 : số phân tử Al2(SO4)3 : số phân tử H2 = 2:3:1:3 |
0,25 |
|
|
d. 2Al + 3Cl2 → 2AlCl3. Số nguyên tử Al : số nguyên tử Cl2 : số phân tử AlCl3 = 2:3:2 |
0,5đ 0,25 |
|
|
Câu 2 (2 điểm) |
3Fe + 2O2 → Fe3O4 Số nguyên tử Fe : số nguyên tử O2 : số phân tử Fe3O4 = 3:2:1
|
0,5đ |
|
0,5đ |
||
|
1 đ |
||
|
|
||
|
Câu 3 (1,0 điểm) |
- Thanh sắt sẽ tăng khối lượng vì có phải ứng với oxi trong không khí. |
1đ |
Tất cả nội dung bài viết. Các em hãy xem thêm và tải file chi tiết dưới đây:
>> Học trực tuyến lớp 8 trên Tuyensinh247.com Học bám sát chương trình SGK mới nhất của Bộ Giáo dục. Cam kết giúp học sinh lớp 8 học tốt, hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
-
Đề kiểm tra 15 phút chương II: Phản ứng hóa học (3 đề - lời giải chi tiết)(22/06)
3 đề kiểm tra 15 phút gồm trắc nghiệm và tự luận với lời giải và thang điểm chi tiết sẽ giúp học sinh củng cố kiến thức đồng thời bổ sung những kiến thức còn thiếu xót
-
Bài tập tự luận phản ứng hóa học (Có lời giải chi tiết)(18/05)
Bài viết tổng hợp các bài tập tự luận với đầy đủ các dạng và được giải chi tiết rõ ràng giúp bạn đọc rèn luyện cách trình bày thật khoa học.
-
30 BTTN lý thuyết phản ứng hóa học (Có đáp án)(18/05)
30 BTTN lý thuyết dưới đây tổng hợp những kiến thức quan trọng của toàn chương giúp bạn đọc nắm vững kiến thức.
-
BTTN tổng hợp chương phản ứng hóa học (Có đáp án)(17/05)
Tổng hợp các bài tập trắc nghiệm dưới đây giúp bạn đọc củng cố lại kiến thức một cách vững chắc.
-
Dấu hiệu phản ứng(17/05)
Khi nào phản ứng hóa học xảy ra? Có những dấu hiệu gì để nhận biết phản ứng hóa học đã xảy ra? Bài viết dưới đây giúp bạn đọc hiểu rõ hơn và làm bài tập thật chính xác.
-
Bài tập viết phương trình hóa học(17/05)
Viết phương trình hóa học là một trong nhưng kỹ năng quan trọng giúp bạn học hóa thật tốt, bài viết dưới đây hướng dẫn bạn đọc cách viết phương trình hóa học một cách đơn giản chính xác.
-
Định luật bảo toàn khối lượng (Đầy đủ - Có bài tập vận dụng cực hay)(16/05)
Đinh luật bảo toàn là một trong những công cụ hữu hiệu giúp giải quyết các bài tập tính toán hóa học một cách hiệu quả. Bài viết này giúp cung cấp những kiến thức căn bản về định luật bảo toàn khối lượng, kèm theo bài tập vận dụng giúp học sinh nắm chắc kiến thức hơn.
-
Lý thuyết về phương trình hóa học (Chi tiết - Có bài tập vận dụng)(16/05)
Phản ứng hóa học được biểu diễn bằng phương trình hóa học. Vậy phương trình hóa học được biểu diễn như thế nào? Hãy cùng tìm hiểu nhé!
-
Phương pháp lập phương trình hóa học (có bài tập vận dụng Cơ bản và nâng cao)(16/05)
Phương trình hóa học thể hiện phản ứng hóa học. Vậy làm thế nào để lập phương trình hóa học một cách chính xác nhất. Các phương pháp hữu hiệu dưới đây sẽ giúp các em giải quyết các bài tập về lập phương trình hóa học từ cơ bản đến nâng caao một cách dễ dàng.
-
Bài tập trọng tâm về phản ứng hóa học(16/05)
Đừng lo lắng khi các bạn không biết xác định đâu là chất tham gia đâu là sản phẩm của phản ứng hóa học, cũng như không biết biểu diễn một phản ứng hóa học ra sao? Hãy cùng nhau tìm hiểu xem phản ứng hóa học có thực sự khó không nhé!