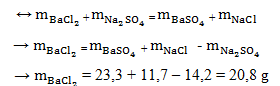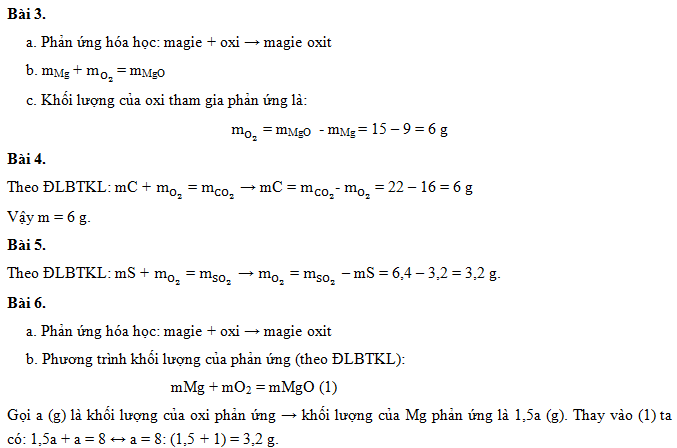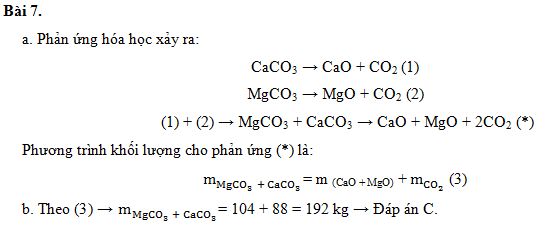Định luật bảo toàn khối lượng (Đầy đủ - Có bài tập vận dụng cực hay)
Cập nhật lúc: 18:40 16-05-2016 Mục tin: Hóa học lớp 8
Xem thêm:
ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG
I. LÝ THUYẾT CẦN NHỚ
1. Định luật bảo toàn khối lượng: “ Trong một phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng của các chất phản ứng”
Giả sử có phản ứng giữa A + B tạo ra C + D có công thức khối lượng được viết như sau :
mA + mB = mC + mD
VD: Bari clorua +natri sunphat bari sunphat + natri clorua. Có CT khối lượng là:
mbari clorua + mnatri sunphat = mbari sunphat + mnatri clorua
2. Áp dụng: trong một phản ứng có n chất, nếu biết khối lượng của (n – 1) chất thì tính được khối lượng của chất còn lại.
II. BÀI TẬP ÁP DỤNG
Bài 1.
a. Phát biểu định luật bảo toàn khối lượng
b. Giải thích vì sao khi một phản ứng hóa học xảy ra, khối lượng các chất được bảo toàn?
Bài 2. Trong phản ứng hóa học : bari clorua + natri sunphat bari sunphat + natri clorua. Cho biết khối lượng của natri sunphat Na2SO4 là 14,2 gam, khối lượng của bari sunphat BaSO4 và natri clorua NaCl lần lượt là : 23,3 g và 11,7 g.
Hãy tính khối lượng của bari clorua BaCl2 đã phản ứng
Bài 3. Đốt cháy hết 9 gam kim loại magie Mg trong không khí thu được 15 g hỗn hợp chất magie oxit MgO. Biết rằng magie cháy là xảy ra phản ứng với oxi O2 trong không khí.
a. Viết phản ứng hóa học trên.
b. Viết công thức về khối lượng của phản ứng xảy ra.
c. Tính khối lượng của khí oxi phản ứng.
Bài 4. Đốt cháy m(g) cacbon cần 16 g oxi thì thu được 22 gam khí cacbonic. Tính m
Bài 5. Đốt cháy 3,2 g lưu huỳnh S trong không khí thu được 6,4 g lưu huỳnh đioxit. Tính khối lượng của oxi đã phản ứng.
Bài 6. Đốt cháy m g kim loại magie Mg trong không khí thu được 8g hợp chất magie oxit (MgO). Biết rằng khối lượng magie Mg tham gia bằng 1,5 lần khối lượng của oxi (không khí) tham gia phản ứng.
a. Viết phản ứng hóa học.
b. Tính khối lượng của Mg và oxi đã phản ứng.
Bài 7. Đá đôlomit (là hỗn hợp của CaCO3 và MgCO3), khi nung nóng đá này tạo ra 2 oxit là canxi oxit CaO và magie oxit MgO và thu được khí cacbon đioxit.
a. Viết phản ứng hóa học xảy ra và phương trình khối lượng nung đá đolomit.
b. Nếu nung đá đôlomit, sau phản ứng thu được 88 kg khí cacbon đioxit và 104 kg hai oxit các loại thì phải dùng khối lượng đá đôlomit là:
A. 150kg B. 16kg C. 192kg D. Kết quả khác.
Bài 8. Hãy giải thích vì sao khi nung thanh sắt thì thấy khối lượng thanh sắt tăng lên, con khi nung nóng đá vôi thấy khối lượng giảm đi.
Bài 9. Hòa tan cacbua canxi (CaC2) vào nước (H2O) ta thu được khí axetylen (C2H2) và canxi hiđroxit (Ca(OH)2).
a. Lập phương trình khối lượng cho quá trình trên.
b. Nếu dùng 41 g CaC2 thì thu được 13 g C2H2 và 37 g Ca(OH)2. Vậy phải dùng bao nhiêu mililit nước? Biết rằng khối lượng riêng của nước là 1g/ ml.
Bài 10. Khi cho Mg tác dụng với axit clohiđric thì khối lượng của magie clorua (MgCl2) nhỏ hơn tổng khối lượng của Mg và axit clohiđric tham gia phản ứng. Điều này có phù hợp với định luật bảo toàn khối lượng không?
Bài 10. Khi cho Mg phản ứng với dung dịch HCl thấy khối lượng MgCl2 nhỏ hơn tổng khối lượng của Mg và HCl. Điều này có phù hợp với định luật bảo toàn khối lượng không? Giải thích.
LỜI GIẢI
Bài 1.
a. “ Trong một phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng của các chất phản ứng”
b. Giải thích: Trong phản ứng hóa học diễn ra sự thay đổi liên kết giữa các nguyên tử. Sự thay đổi này chỉ liên quan đến electron, còn số nguyên tử mỗi nguyên tố vẫn giữ nguyên và khối lượng nguyên tử không đổi. Do đó khối lượng các chất được bảo toàn.
Bài 2.
Áp dụng định luật bảo toàn khối lượng (BTKL)
mbari clorua + mnatri sunphat = mbari sunphat + mnatri clorua
Bài 8.
Khi nung thanh sắt có khối lượng tăng vì ở nhiệt độ cao sắt tác dụng với oxi tạo thành sắt oxit.
Khi nung nóng đá vôi thấy khối lượng giảm đi vì khi nung đá vôi tạo ra vôi sống và khí CO2 (khí CO2 là khí ở nhiệt độ cao dễ dàng thoát ra ngoài), chỉ còn lại vôi sống nên khối lượng giảm so với ban đầu.
Tất cả nội dung bài viết. Các em hãy xem thêm và tải file chi tiết dưới đây:
>> Học trực tuyến lớp 8 trên Tuyensinh247.com Học bám sát chương trình SGK mới nhất của Bộ Giáo dục. Cam kết giúp học sinh lớp 8 học tốt, hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
-
Đề kiểm tra 15 phút chương II: Phản ứng hóa học (3 đề - lời giải chi tiết)(22/06)
3 đề kiểm tra 15 phút gồm trắc nghiệm và tự luận với lời giải và thang điểm chi tiết sẽ giúp học sinh củng cố kiến thức đồng thời bổ sung những kiến thức còn thiếu xót
-
Đề kiểm tra 45 phút chương II: Phản ứng hóa học(21/06)
Bài viết giúp học sinh rèn luyện kĩ năng giải quyết vấn đề hóa học, đồng thời giúp học sinh đánh giá được năng lực học hóa học của bản thân để có phương pháp học tập thích hợp
-
Bài tập tự luận phản ứng hóa học (Có lời giải chi tiết)(18/05)
Bài viết tổng hợp các bài tập tự luận với đầy đủ các dạng và được giải chi tiết rõ ràng giúp bạn đọc rèn luyện cách trình bày thật khoa học.
-
30 BTTN lý thuyết phản ứng hóa học (Có đáp án)(18/05)
30 BTTN lý thuyết dưới đây tổng hợp những kiến thức quan trọng của toàn chương giúp bạn đọc nắm vững kiến thức.
-
BTTN tổng hợp chương phản ứng hóa học (Có đáp án)(17/05)
Tổng hợp các bài tập trắc nghiệm dưới đây giúp bạn đọc củng cố lại kiến thức một cách vững chắc.
-
Dấu hiệu phản ứng(17/05)
Khi nào phản ứng hóa học xảy ra? Có những dấu hiệu gì để nhận biết phản ứng hóa học đã xảy ra? Bài viết dưới đây giúp bạn đọc hiểu rõ hơn và làm bài tập thật chính xác.
-
Bài tập viết phương trình hóa học(17/05)
Viết phương trình hóa học là một trong nhưng kỹ năng quan trọng giúp bạn học hóa thật tốt, bài viết dưới đây hướng dẫn bạn đọc cách viết phương trình hóa học một cách đơn giản chính xác.
-
Lý thuyết về phương trình hóa học (Chi tiết - Có bài tập vận dụng)(16/05)
Phản ứng hóa học được biểu diễn bằng phương trình hóa học. Vậy phương trình hóa học được biểu diễn như thế nào? Hãy cùng tìm hiểu nhé!
-
Phương pháp lập phương trình hóa học (có bài tập vận dụng Cơ bản và nâng cao)(16/05)
Phương trình hóa học thể hiện phản ứng hóa học. Vậy làm thế nào để lập phương trình hóa học một cách chính xác nhất. Các phương pháp hữu hiệu dưới đây sẽ giúp các em giải quyết các bài tập về lập phương trình hóa học từ cơ bản đến nâng caao một cách dễ dàng.
-
Bài tập trọng tâm về phản ứng hóa học(16/05)
Đừng lo lắng khi các bạn không biết xác định đâu là chất tham gia đâu là sản phẩm của phản ứng hóa học, cũng như không biết biểu diễn một phản ứng hóa học ra sao? Hãy cùng nhau tìm hiểu xem phản ứng hóa học có thực sự khó không nhé!